
400-0355-662
制造商,进口商,重贴标签商,重包装商,哪些要求向FDA支付年费,进行注册列示?
参与生产和分销用于美国商业分销的医疗器械的机构,包括那些仅为出口而进口的医疗器械,必须每年向FDA注册。大多数需要注册的机构还需要列出该机构的设备和在这些设备上执行的活动。对于我们国内的医疗器械制造商,产品要在美国销售的,可能有些朋友是搞不清楚自己或者自己的合作方需不需要在FDA进行注册活动的。
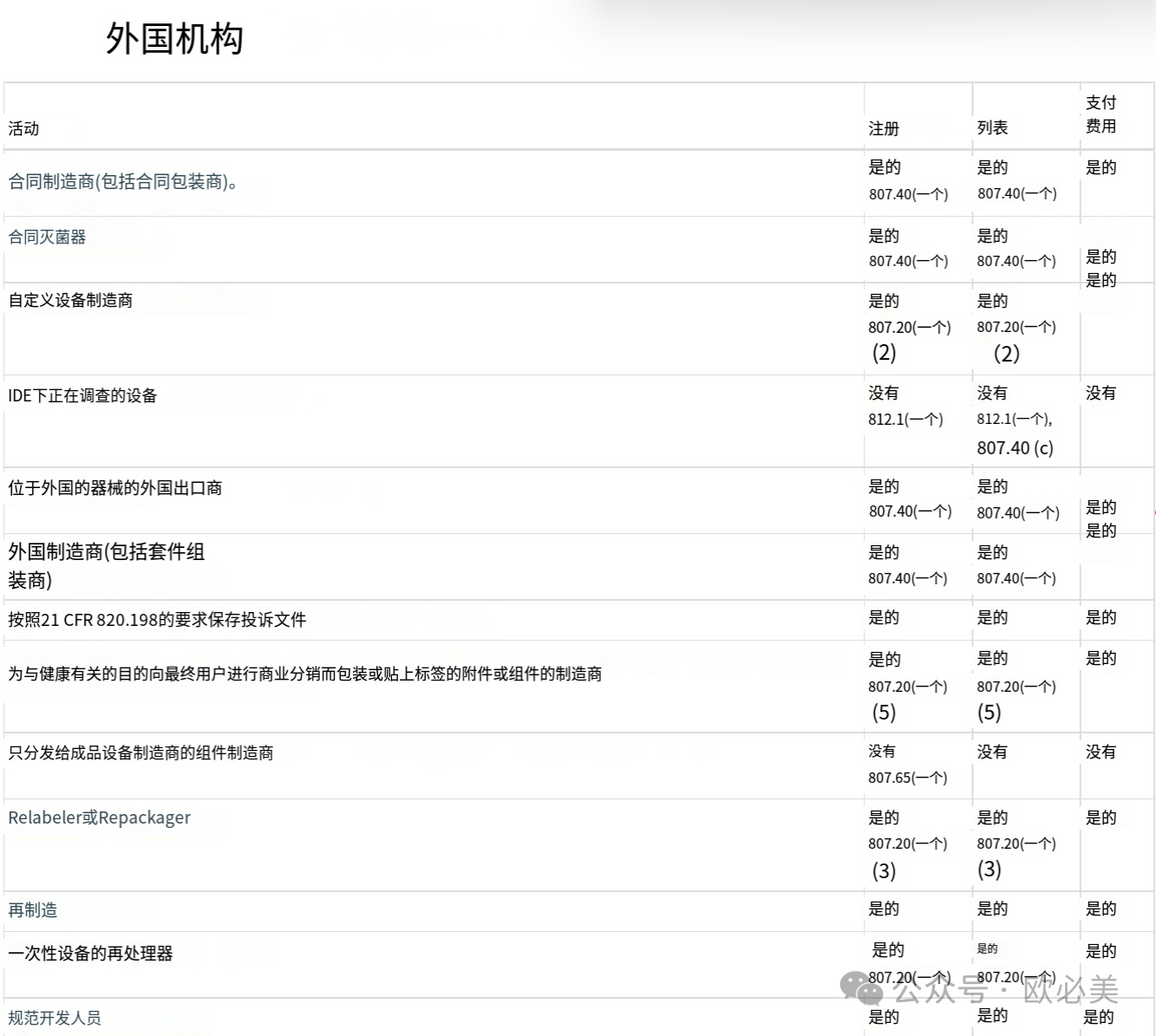
下面小欧根据该企业进行的活动类型列出了注册和上市的要求。
一、介绍机构活动的相关定义
合约制造商 (Contract Manufacturer):
根据另一机构的规格生产成品器械。
合约灭菌方 (contract Sterilizer):
为其他机构的器械提供灭菌服务。
国外出口商 (Foreign Exporter):
向美国出口或提供向美国出口在国外制造、制备、合成或加工的器械,包括最初在美国制造的器械。国外出口商必须在美国以外有营业地址。
初始进口商 (Initial Importer):
任何将器械从外国制造商进一步营销到最终交付或销售器械给最终消费者或用户的人的进口商,但不重新包装,或以其他方式改变器械或器械包装的容器,包装或标签。初始进口商必须在美国有一个实际地址,由负责确保进口器械符合所有适用的FDA法律法规的人员配备。
制造商 (Manufacturer):
通过化学、物理、生物或其他程序制造的任何物品符合《联邦食品、药品和药品管理条例》第201(h)节中“器械”的定义化妆品(FD&C)法案。
重新包装商 (Repackager):
通过化学、物理、生物或其他程序制造的任何物品符合《联邦食品、药品和药品管理条例》第201(h)节中“器械”的定义化妆品(FD&C)法案。。
重新贴牌商 (Relabeler):
改变标签内容,把其他制造商生产的产品以自己的名义销售。重新贴标签者不包括不改变原来的标签,而只是添加自己的名称的机构。
再制造商 (Remanufacturer):
对成品器械进行加工、处理、翻新、重新包装、恢复或做出任何其他行为,显著改变成品器械的性能或安全规格或预期用途的人。
对一次性器械再处理 (Reprocessor of Single Use Device):
在一次性器械上执行再制造操作。
规范开发人员 (Specification Developer):
开发器械的规范,该器械以公司自己的名义分发,但不进行制造。这包括企业,除了制定规范外,还安排由合同制造商以另一家企业的名义生产器械。

二、参考网站
https://www.fda.gov/medical-devices/device-registration-and-listing/who-must-register-list-and-pay-fee
版权所有© 2023 欧必美(青岛)医疗技术有限公司 备案号:XXXX 技术支持:苏州慕名
扫描二维码分享到微信