
400-0355-662
沙特多个器械注册捆绑原则
沙特医疗器械领域的监管机构沙特食品药品监督管理局(SFDA)发布了一份指导文件,专门介绍了在沙特阿拉伯王国销售和使用的医疗器械捆绑/分组的方法。该文件描述了适用于上述目的的特定标准,并就相关监管要求提供了额外的澄清和建议。
本SFDA指南旨在为医疗器械制造商和参与医疗器械运营的其他各方提供关于在单一医疗器械营销授权(MDMA)申请程序中捆绑/分组医疗器械的标准的额外澄清。在某些方面,本文件还参考了SFDA早些时候发布的关于上市授权的指南。
如果有必要在单个应用程序中对一种以上的医疗器械类型进行分组,则应采用本SFDA指南中描述的方法。因此,申请人MDMA可以在一个申请程序中对一种以上的医疗器械类型进行分组。SFDA还提到,如果相关实体(医疗器械制造商或其授权代表)提交的申请范围涵盖不同用途或具有不同分类或技术性能的医疗器械,监管机构将要求申请人提供额外信息,因此可能会提出大量请求。SFDA 要求提供的实际信息范围将根据相关医疗器械的类型而有所不同。
医疗器械(非IVD)捆绑类型分为3种:
01
医疗器械家族
02
医疗器械系统
03
医疗设备程序包
该文件还详细描述了上述每种类型。
“医疗器械家族”的概念代表由同一医疗器械制造商生产的一组医疗器械,前提是所有器械都是同一时间,但具有不同的形状和特征。同时,这些设备也应具有相同的预期用途。为了被允许应用这种方法,申请人应确保满足以下所有标准——进行分组的医疗器械应:
根据目前的SFDA指南,“医疗器械系统”包括多个组成部分,以完成共同的预期目的。为了符合资格,医疗器械系统应具有相同的制造商,并且最初旨在完成共同的预期目的。它也应该以一个通用名称投放市场,并贴上相应的标签。在申请医疗器械系统注册时,申请人应根据分配给最高级别组件的级别来确定级别。最初打算与系统内的设备一起使用的附件也可以在同一应用程序中注册。
根据该指南,”医疗器械程序包”代表制造商将两个或多个医疗器械组装在一起,作为一个包执行特定程序的集合。该文件还概述了适用的适当资格标准。
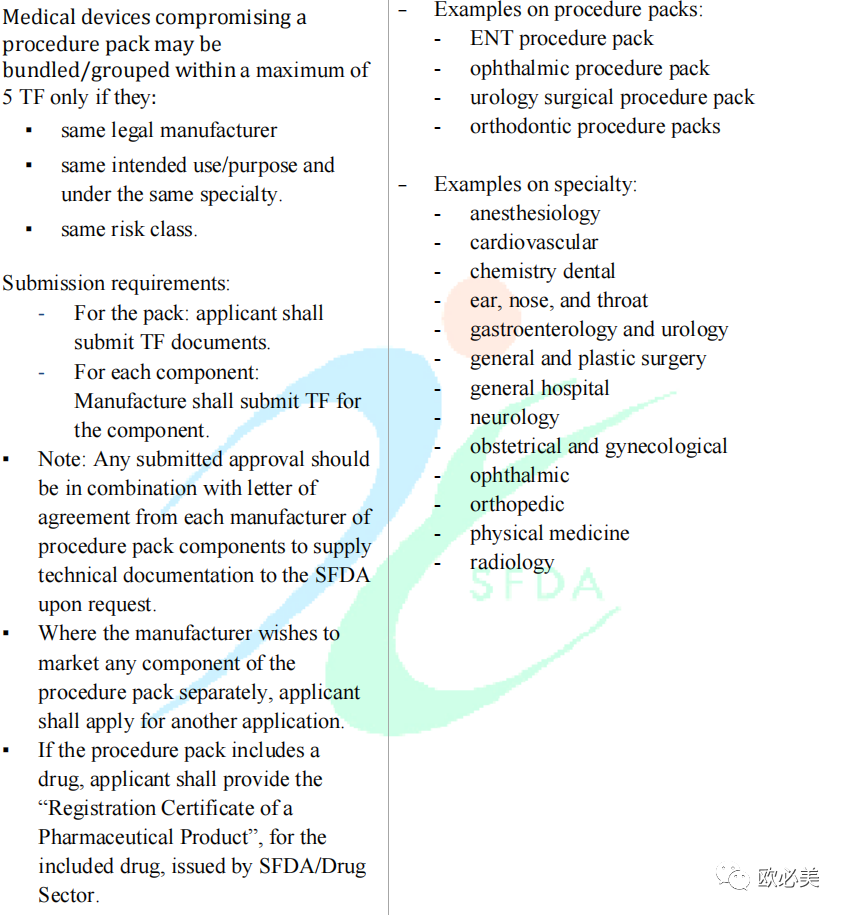
总之,SFDA指南详细描述了在确定有兴趣将其产品投放到本国市场的一方提交的申请的分组类型的资格时应适用的规则。特别是,该文件描述了主要类型的应用程序,并强调了在这方面需要考虑的最重要方面。
版权所有© 2023 欧必美(青岛)医疗技术有限公司 备案号:XXXX 技术支持:苏州慕名
扫描二维码分享到微信